Am 11. März 2020 erklärte die Weltgesundheitsorganisation den Ausbruch von COVID-19 (SARS-CoV-2) zu einer Pandemie ( ). Bis zum 30. März 2020 wurde COVID-19 in 177 Ländern/Regionen bestätigt, hat über 730.000 Menschen infiziert und mehr als 34.000 Todesopfer gefordert (Quelle: JHU). Während die meisten der mit dem Virus infizierten Menschen nur leichte Symptome zeigen, gehen Experten davon aus, dass ältere Erwachsene und Menschen mit Grunderkrankungen wie Herz-Kreislauf-Erkrankungen, Diabetes, chronischen Atemwegserkrankungen und Krebs ein höheres Risiko haben.
Derzeit gibt es kein spezifisches Medikament zur Behandlung oder Vorbeugung von COVID-19, aber viele industrielle, akademische und staatliche Einrichtungen arbeiten mit Hochdruck an der Entwicklung wirksamer Behandlungsmöglichkeiten. Auch wenn ein Impfstoff noch eine Weile auf sich warten lässt, werden bereits zugelassene kleine Moleküle bei schwerkranken Patienten eingesetzt. Weitere Möglichkeiten bieten neu entwickelte Biologika, die auf andere Coronaviren abzielen, sowie experimentelle Therapeutika, wie z. B. siRNA-basierte Therapeutika. Jüngste Durchbrüche wie die Sequenzierung des SARS-CoV-2-Virus haben eine Reihe von Unternehmen in die Lage versetzt, Testkits zu entwickeln und den Forschern wichtige Daten für die Entwicklung einer Behandlung zu liefern.
In der Zwischenzeit ergreifen die Regierungen auch andere Gegenmaßnahmen, um die Ausbreitung der Infektion einzudämmen. Zu diesen Maßnahmen gehören Ankündigungen des öffentlichen Gesundheitswesens in Bezug auf soziale Distanzierung und Händewaschen, die Isolierung kranker Patienten, die Schließung nicht lebensnotwendiger Geschäfte und in einigen Fällen die Quarantäne ganzer Gemeinden.
Seit Bekanntwerden des Ausbruchs hat die US-amerikanische Gesundheitsbehörde FDA mehrere Maßnahmen zur Bewältigung der Pandemie ergriffen. Sie hat auch die erweiterte Verwendung von Medizinprodukten und eine Liste von Diagnosekits im Rahmen ihres Emergency Use Authorization (EUA)-Programms genehmigt. Gemäß Abschnitt 564 des Federal Food, Drug, and Cosmetic Act (FD&C Act) kann der FDA-Kommissar nicht zugelassene Medizinprodukte oder nicht zugelassene Verwendungen zugelassener Medizinprodukte in Notfällen zur Diagnose, Behandlung oder Vorbeugung schwerer oder lebensbedrohlicher Krankheiten zulassen, wenn es keine angemessenen, zugelassenen und verfügbaren Alternativen gibt.
Einer der Gründe, warum COVID-19 eine Herausforderung darstellt, ist die Tatsache, dass das Virus von Personen, die keine Symptome aufweisen, auf andere übertragen werden kann. Aus diesem Grund wurde großer Wert auf die Entwicklung und den Einsatz von In-vitro-Diagnosekits (IVD) und Point-of-Care-Geräten gelegt. Eine frühzeitige Erkennung ist der Schlüssel zur Eindämmung der Ausbreitung der Infektion. In der nachstehenden Tabelle 1 sind 20 IVD aufgeführt, die von der FDA im Rahmen des EUA ab dem 27. März 2020 zugelassen wurden. Die frühesten Zulassungen betrafen Geräte, die vom Center for Disease Control and Prevention (CDC) und dem Wadsworth Center - beides Regierungsbehörden - hergestellt wurden. Im Anschluss an diese Zulassungen wurde am 12. März der cobas SARS-CoV-2 von Roche - ein Dual-Target-Assay mit einer Vertiefung - zugelassen, die erste Zulassung für einen privaten Anbieter.
| Datum der Ausgabe | Bausatz | Antragsteller | Kategorie |
|
04-Feb-20 |
CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR |
CDC |
EUA |
| 29-Feb-20 | SARS-CoV-2-Echtzeit-RT-PCR-Diagnosepanel | Wadsworth Center, NYSDOH | EUA |
| 12-Mär-20 | cobas SARS-CoV-2-Test | Roche Molekulare Systeme | EUA |
| 13-Mär-20 | TaqPath COVID-19-Kombinationssatz | Thermo Fisher | EUA |
| 16-Mär-20 | COVID-19 RT-PCR-Test | LabCorp | EUA |
| 16-Mär-20 | Panther Fusion SARS-CoV-2 | Hologic, Inc. | EUA |
| 17-Mär-20 | Quest SARS-CoV-2 rRT-PCR Test | Quest Diagnostik | EUA |
| 17-Mär-20 | Lyra SARS-CoV-2-Assay | Quidel Gesellschaft | EUA |
| 18-Mär-20 | Abbott RealTime SARS-CoV-2-Test | Abbott Molekular | EUA |
| 19-Mär-20 | ePlex SARS-CoV-2 Test | GenMark Diagnostics, Inc. | EUA |
| 19-Mär-20 | Simplexa COVID-19 Direkter Test | DiaSorin Molecular LLC | EUA |
| 20-Mär-20 | Xpert Xpress SARS-CoV-2 Test | Cepheid | EUA |
| 20-Mär-20 | COVID-19 genesig Real-Time PCR-Assay | Primerdesign GmbH | EUA |
| 23-Mär-20 | Accula SARS-Cov-2 Test | Mesa Biotech Inc. | EUA |
| 23-Mär-20 | BioFire COVID-19-Test | BioFire Defense, LLC | EUA |
| 24-Mär-20 | PerkinElmer Neues Nukleinsäure-Nachweiskit für Coronaviren | PerkinElmer, Inc. | EUA |
| 25-Mär-20 | AvellinoCoV2-Test | Avellino Lab USA, Inc. | EUA |
| 26-Mär-20 | Fluoreszenz-RT-PCR-Kit für den Echtzeit-Nachweis von SARS-2019-nCoV | BGI Genomics Co. Ltd. | EUA |
| 27-Mär-20 | ID JETZT COVID-19 | Abbott Diagnostics Scarborough, Inc. | EUA |
| 27-Mär-20 | NxTAG CoV Erweiterter Panel-Assay | Luminex Molekulare Diagnostik GmbH | EUA |
Tabelle 1: Liste der von der FDA zugelassenen In-vitro-Diagnostika unter EUA
Interessant ist, dass die Patentanmeldungen im Zusammenhang mit In-vitro-Diagnostika im Zusammenhang mit Coronaviren nach früheren Pandemien einen Höhepunkt erreichten (Abbildung 1). Der Höhepunkt der Patentanmeldungen in den Jahren 2003-2004 resultierte nach dem SARS-Ausbruch im Jahr 2003. Der Höhepunkt der Patentanmeldungen in den Jahren 2013 und 2016 folgte auf den MERS-Ausbruch im Jahr 2012. Wir können einen ähnlichen unmittelbaren Anstieg der Patentanmeldungen im Jahr 2020 erwarten, da bereits mehrere kommerzielle Kits eingeführt wurden und weitere wahrscheinlich auf dem Weg sind.
Die meisten Innovationen im Bereich der Diagnostik haben ihren Ursprung in den USA, haben aber in verschiedenen Ländern der Welt kommerzielles Potenzial gefunden. Die Patentanmeldungen deuten auf eine starke Dominanz von Unternehmen mit Sitz in den USA in der globalen Patentlandschaft hin. Der asiatisch-pazifische Raum, einschließlich China, Japan, Südkorea und Hongkong, weist ebenfalls bedeutende Erstanmeldungen auf, die auf die früheren Ausbrüche in der Region zurückzuführen sind.
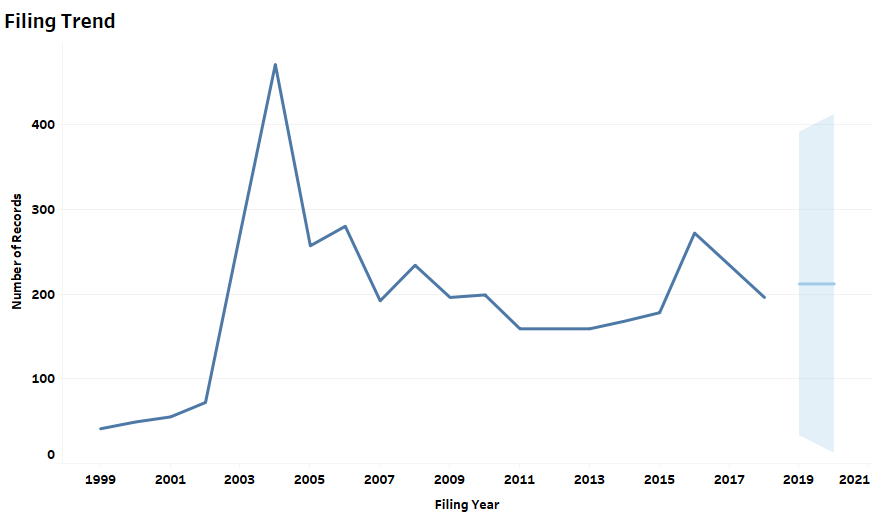
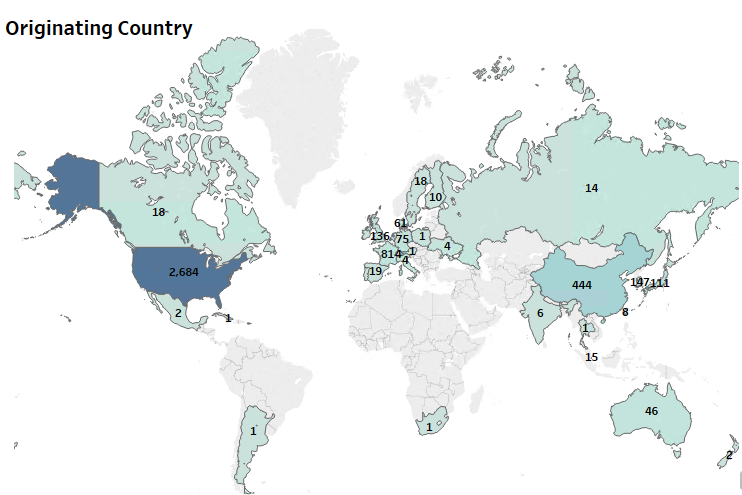
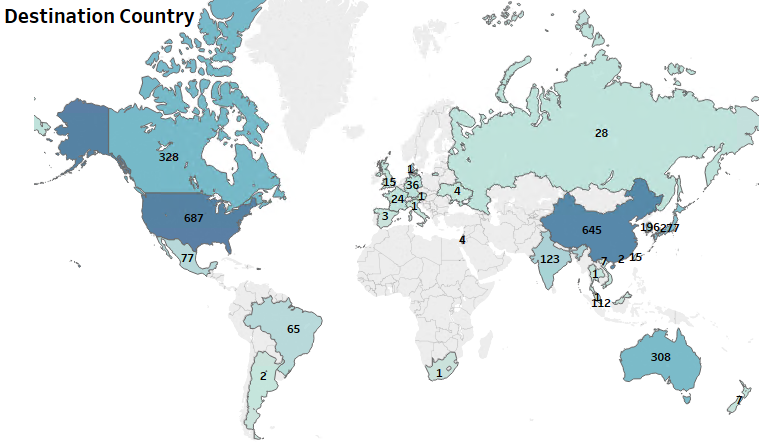
Abbildung 1: Patent-Dashboard mit Darstellung des Anmeldetrends im Zusammenhang mit Diagnostika, den Ländern mit der höchsten Innovationsrate und den Marktgerichtsbarkeiten für die Tests
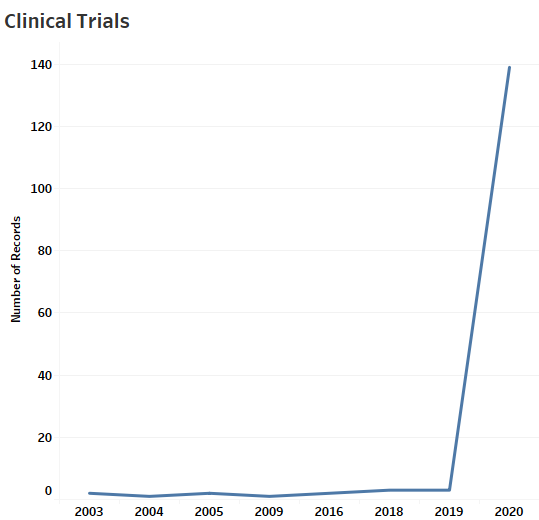
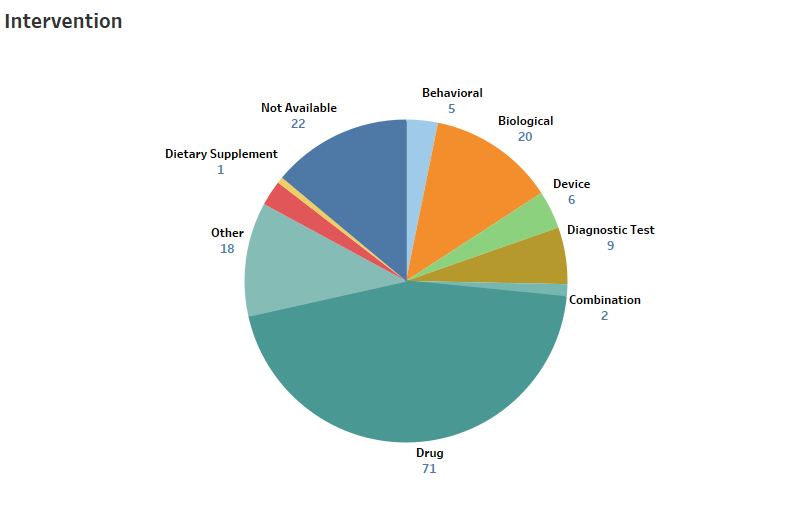
MaxVal ermittelte insgesamt 158 offene und abgeschlossene klinische Studien (Abbildung 2) zum Coronavirus, von denen die meisten offenbar als Reaktion auf die aktuelle SARS-CoV-2-Pandemie eingeleitet wurden. In diesen Studien werden anscheinend am häufigsten therapeutische Maßnahmen untersucht. Neun der 158 Studien betreffen diagnostische Tests. Eine davon bezieht sich auf die Verwendung des VivaDiag SARS-CoV-2 IgM/IgG-Schnelltests. Eine weitere bezieht sich auf den Einsatz von Lungenultraschall zur Erkennung. Eine dritte Studie befasst sich mit einer neuen vollautomatischen QIAstat-Dx-Plattform für den multiplen PCR-Nachweis. Es ist bemerkenswert, dass die Zahl der klinischen Studien zum Zeitpunkt der früheren MERS- und SARS-Ausbrüche verschwindend gering war. Vielleicht waren die Lehren aus der Vergangenheit lehrreich.
Abbildung 2: Das Dashboard für klinische Studien zeigt die Anzahl der Studien und die Art der Intervention für alle zugehörigen Studien (Stand: 25. März 2020)
Die Datenanalyse von MaxVal zeigt, dass die Zahl der Patente, Veröffentlichungen und klinischen Studien im Zusammenhang mit der Bekämpfung von COVID-19 in naher Zukunft exponentiell ansteigen wird. In der Zwischenzeit sind unsere derzeit besten Strategien zur Minimierung der Auswirkungen von COVID-19 nach wie vor frühzeitige Tests, körperliche Distanzierung, häufiges Händewaschen und Isolierung bei Auftreten von Symptomen.
Werfen Sie einen Blick auf unsere frühere Berichterstattung über den Ausbruch des Coronavirus hier.
Um mehr über die Suchdienste von MaxVal zu erfahren, klicken Sie bitte hier.