Kite Pharma, eine Tochtergesellschaft von Gilead Sciences, hat kürzlich beim Federal Circuit Berufung gegen ein früheres Urteil zugunsten von Juno Therapeutics (Juno), dem Memorial Sloan Kettering Cancer Center und dem Sloan Kettering Institute for Cancer Research Center eingelegt (Fallnummer: 2020-1758).
Kite Pharma wird von Munger, Tolles & Olson und Fish and Richardson vertreten. Juno wird von Irell and Manella LLP und Jones Day vertreten.
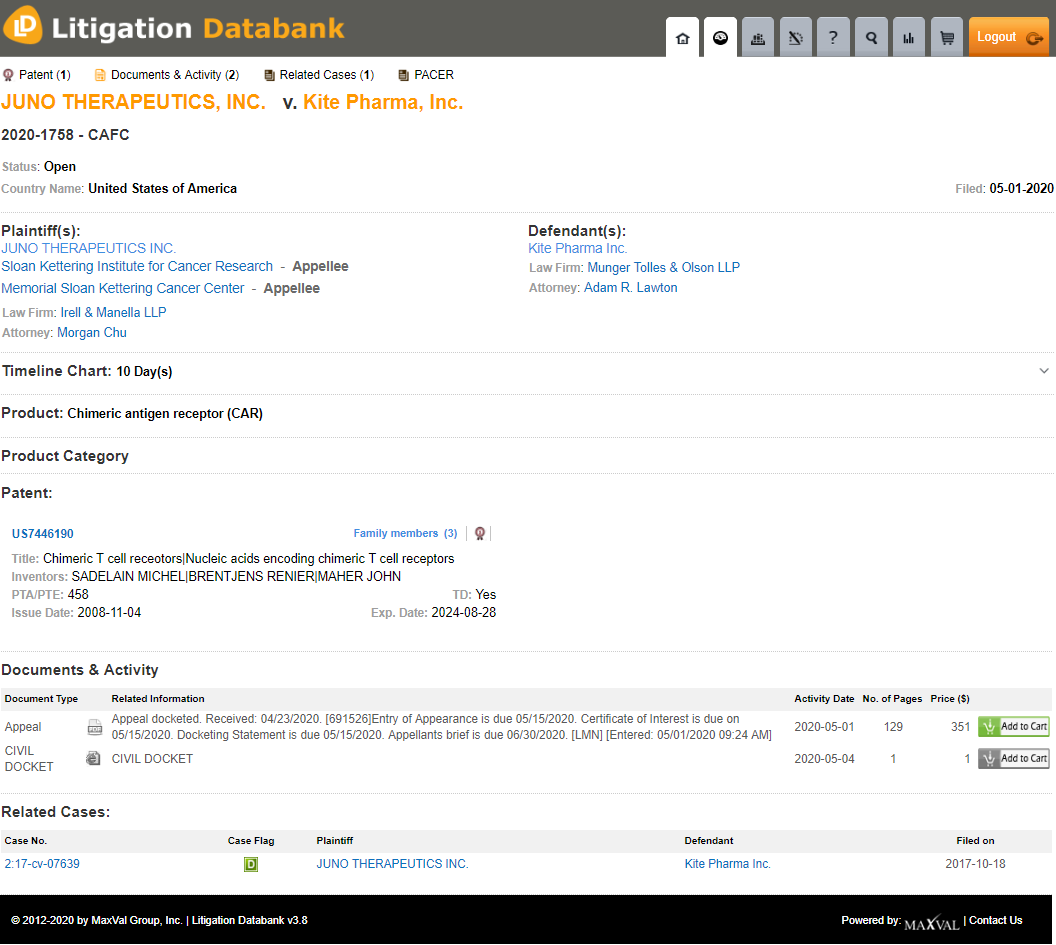
Quelle: MaxVal's Rechtsstreit-Datenbank
Das Patent 7.446.190, um das es in diesem Fall geht, bezieht sich auf Verfahren zur Verwendung chimärer T-Zell-Rezeptoren, um die T-Zell-Antwort auf ein bestimmtes Ziel zu erleichtern. Der ursprüngliche Rechtsnachfolger, das Sloan-Kettering Institute For Cancer Research, erteilte Juno Therapeutics am 21. November 2013 eine Exklusivlizenz für diese Technologie. Juno Therapeutics ist ein Unternehmen von Bristol-Myers Squibb, das die Muttergesellschaft von Juno, Celgene, übernommen hat.
In dem früheren Urteil stellte das zentrale Bezirksgericht von Kalifornien fest, dass Kite Pharma vorsätzlich die Ansprüche 3, 5, 9 und 11 des US-Patents 7.446.190 von Juno durch den Verkauf der CAR-T-Therapie (Chimeric Antigen Receptor T-Cell) von Kite Pharma verletzt hat. Die Gegenklage von Kite Pharma auf Nichtverletzung und Ungültigkeit der Ansprüche wurde vom Gericht abgewiesen. Darüber hinaus wurde der von den Geschworenen zuerkannte Schadenersatz von 752 Millionen US-Dollar vom Gericht auf rund 1,2 Milliarden US-Dollar erhöht (Aktenzeichen: 2:17-cv-07639).
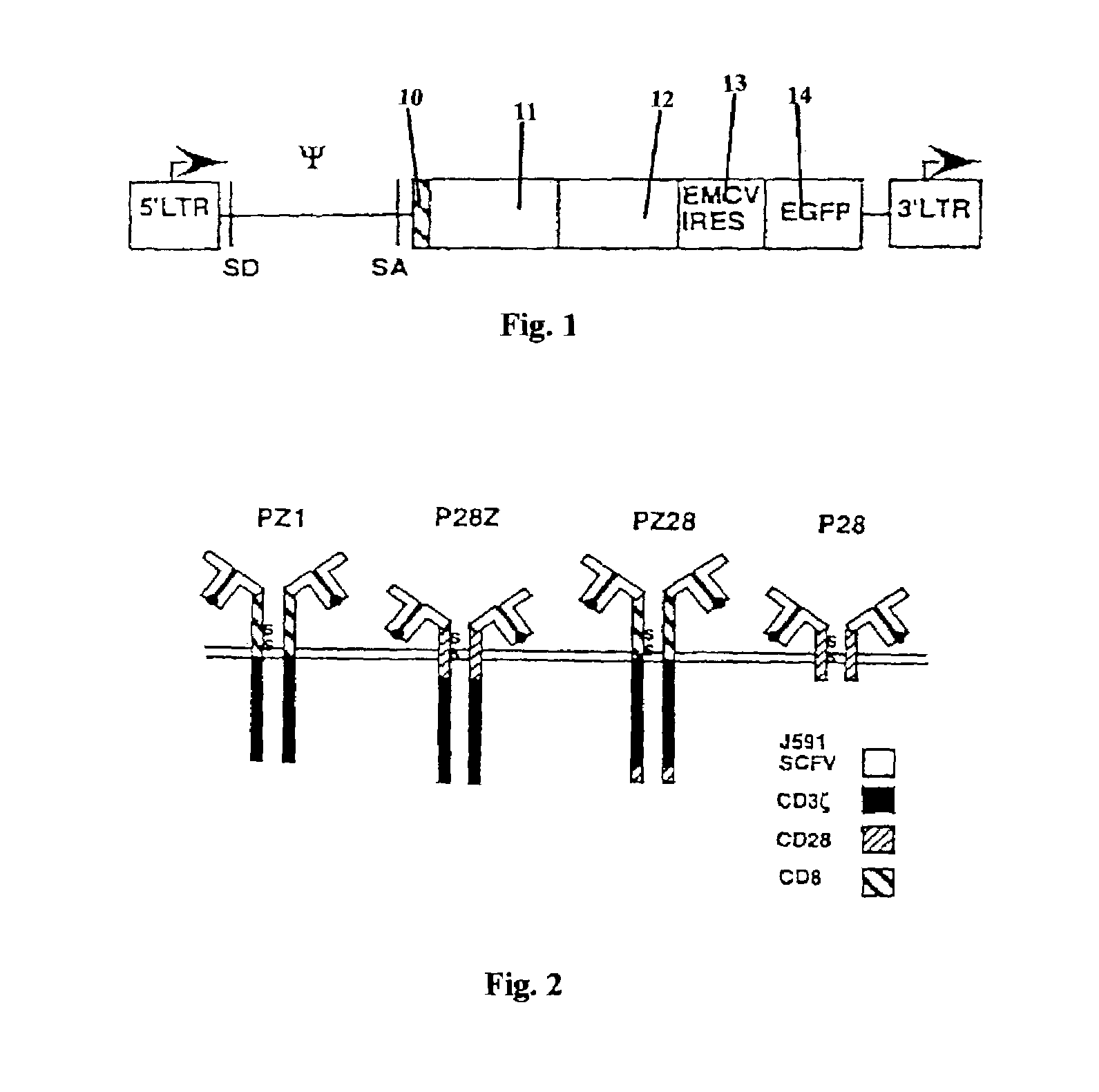
Das US-Patent 7,446,190 von Juno bezieht sich auf eine CAR-T-Zelle, die für drei spezifische Elemente kodiert: 1) ein antigenbindendes Molekül gegen ein Ziel wie CD19; 2) eine co-stimulatorische CD28-Domäne; und 3) eine intrazelluläre CD3ζ-Domäne. Sobald die CAR-T-Zelle an das Ziel gebunden ist, sendet das CD3ζ-Element Signale, um die anvisierte Krebszelle zu töten. Die Hinzufügung eines ko-stimulatorischen Signals wie CD28 kann die T-Zell-Aktivierung sowie die Persistenz und Wirksamkeit von CAR-T-Therapien verbessern.
Yescarta (Axi-cel oder Axicabtagene ciloleucel) ist eine CAR-T-Therapie, die ursprünglich in der chirurgischen Abteilung des National Cancer Institute (NCI) entwickelt und später zur weiteren Entwicklung an Kite Pharma lizenziert wurde. Yescarta ist eine von der US FDA zugelassene Behandlung für rezidivierte oder refraktäre großzellige B-Zell-Lymphome bei Erwachsenen. Bei dem Medikament handelt es sich um eine personalisierte autologe T-Zell-Therapie, die dem Patienten per Infusion verabreicht wird. Eine Behandlung mit dem Medikament kostet 373.000 $. Der Umsatz von Kite Pharma mit Yescarta belief sich 2019 auf 456 Millionen US-Dollar gegenüber 264 Millionen US-Dollar im Jahr 2018, was weniger ist als der vom Gericht festgesetzte Schadenersatz in Höhe von 1,2 Milliarden US-Dollar. Vermutlich hat das Gericht den Schadensersatzbetrag aufgrund seiner Einschätzung der Vorsätzlichkeit der Rechtsverletzung durch Kite Pharma erhöht. Sofern Kite Pharma seine Berufung nicht gewinnt, werden seine Gewinnspannen aufgrund des zugesprochenen Schadenersatzes und einer laufenden Lizenzgebühr von 27,6 % auf die Nettoeinnahmen aus künftigen Verkäufen von Yescarta schrumpfen.
Die CAR-T-Therapien sind ein heiß umkämpftes Gebiet mit mehreren strittigen Patenten. Interessanterweise befindet sich der CAR-T-Kandidat KTE-X19 von Kite Pharma zur Behandlung erwachsener Patienten mit rezidiviertem oder refraktärem Mantelzell-Lymphom (MCL) in der Prioritätsprüfung durch die FDA. KTE-X19 hat das gleiche Konstrukt wie Axi-cel von Yescarta, unterscheidet sich aber im Herstellungsprozess, da KTE-X19 eine spezifische T-Zell-Selektion und Lymphozytenanreicherung beinhaltet, die für die Aktivität gegen bestimmte B-Zell-Malignome erforderlich ist.
Der Wirkstoffkandidat von Bristol-Myers Squibb, Lisocabtagene Maraleucel (Liso-Cell), wird ebenfalls im Rahmen eines beschleunigten Zulassungsverfahrens für die Behandlung von erwachsenen Patienten mit rezidiviertem oder refraktärem (R/R) großzelligem B-Zell-Lymphom geprüft. Sein CAR-T-Konstrukt umfasst ein Anti-CD19-Einzelketten-Variables Fragment (scFv) als Zielbereich für die Antigenspezifität, einen Transmembranbereich und einen 4-1BB-kostimulatorischen Bereich.
Setzen Sie sich mit uns in Verbindung, um ein Exemplar eines Landschaftsberichts über die CAR-T-Therapie anzufordern. Erfahren Sie mehr über unsere Suchdienste für Validität und Validität.
Lassen Sie uns wissen, was Sie in unserem nächsten Blog/Webinar sehen möchten. Nehmen Sie an der Leserumfrage teil